Kemiske målinger
Indledning
Kemiske målinger er grundlaget for at forstå og kontrollere kemiske processer i både laboratorier, industri og miljøovervågning. De bruges til at bestemme egenskaber som surhedsgrad, koncentration, ionstyrke og sammensætning af forskellige opløsninger. Præcise kemiske målinger sikrer, at processer forløber korrekt, produkter har den ønskede kvalitet, og miljøkrav overholdes.
Et centralt område inden for kemiske målinger er bestemmelse af pH, som angiver surhedsgraden i en opløsning. pH-værdien kan påvirke kemiske reaktioner, biologiske processer og materialers stabilitet. Til måling anvendes pH-metre, der består af en elektrode og et måleinstrument. Elektroden reagerer på koncentrationen af hydrogenioner i opløsningen og omdanner dette til et elektrisk signal, som pH-meteret viser som en numerisk værdi.
Udover pH-målinger er koncentrationsmålinger af opløste stoffer essentielle. Kemiske opløsninger kan indeholde både enkle ioner og komplekse forbindelser, og præcis bestemmelse af deres koncentration er nødvendig for kemiske analyser, kvalitetskontrol og forskning. Koncentrationsmålinger udføres typisk ved titrering, spektroskopi eller elektrokemiske metoder, hvor signalet relateres til mængden af stoffet i opløsningen.
Sammenfattende gør kemiske målinger det muligt at kontrollere og optimere kemiske processer, sikre korrekt pH og koncentrationer, og dermed skabe pålidelige og reproducerbare resultater på tværs af laboratorier, industri og miljøanalyser.

pH-måling
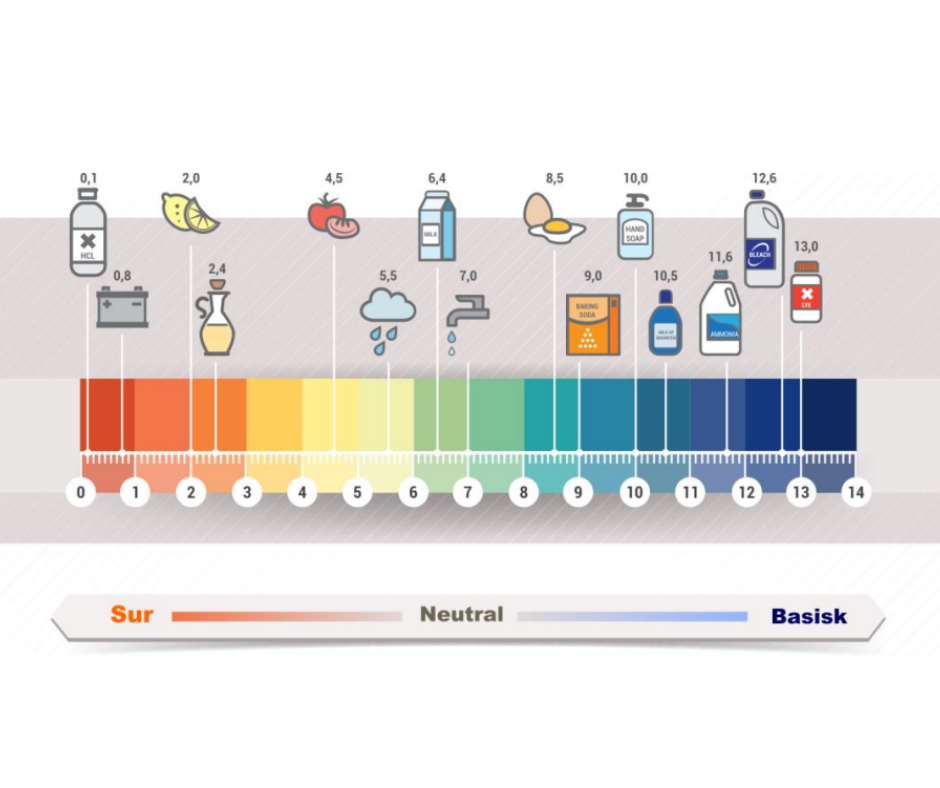
pH-måling er en af de mest anvendte kemiske målinger og bruges til at bestemme surhedsgraden eller basiskheden i væsker. pH-skalaen går typisk fra 0 til 14, hvor lave værdier angiver stærke syrer, og høje værdier angiver stærke baser. I dagligdagen møder vi syrer i mavesækken, i fødevarer som frugtjuice og marinerede sild, samt i husholdningsprodukter som eddike. Baser, derimod, smager ludagtigt eller sæbeagtigt og findes blandt andet i rengøringsmidler og visse fødevarer.
pH er afgørende for mange processer, hvor vand indgår. I biologiske systemer er tolerancen ofte meget snæver, eksempelvis skal blodets pH ligge mellem 7,35 og 7,45 for at opretholde livsvigtige funktioner. Selv små afvigelser kan være farlige. Derfor er præcis pH-måling kritisk i både medicinske og industrielle sammenhænge.
I produktion og fødevareindustrien sikrer pH-kontrol korrekte resultater, fx at marmelade stivner korrekt, mælk ikke bliver sur, og ost får den ønskede konsistens og smag. pH-målinger udføres typisk med pH-metre, der består af en elektrode, som registrerer koncentrationen af hydrogenioner i opløsningen og omdanner dette til en numerisk værdi. Gennem nøjagtig pH-måling kan både biologiske, kemiske og industrielle processer styres effektivt og sikkert.
pH-metre

pH-metre er moderne instrumenter til bestemmelse af surhedsgrad i væsker og anvender primært elektrokemiske målemetoder. Hvor man tidligere brugte indikatorpapir eller naturlige indikatorer som rødkålssaft, måler pH-metre nu direkte via en elektrokemisk celle. Denne celle fungerer på samme princip som et elektrisk batteri og omdanner koncentrationen af hydrogenioner i opløsningen til en elektrisk spænding. Spændingen aflæses derefter af pH-meteret og omdannes til en pH-værdi.
Metoden, der anvendes i moderne pH-metre, kaldes potentiometrisk måling. Her afhænger målesignalet direkte af aktivitet eller koncentration af hydrogenioner, hvilket gør målingen både præcis og reproducerbar. pH-metre består typisk af en elektrode, ofte en glas- eller kombinatorelektrode, og et måleinstrument, som aflæser spændingen og viser den som en numerisk pH-værdi.
Fordelen ved pH-metre er, at de giver langt mere nøjagtige og hurtige målinger end traditionelle indikatorer. De kan anvendes i både laboratorier, industrien og feltmålinger, hvor præcision er afgørende. Potentiometriske pH-målinger gør det muligt at overvåge og kontrollere kemiske, biologiske og industrielle processer effektivt, hvor korrekt surhedsgrad er nødvendig for både kvalitet, sikkerhed og funktion.
Kemiske opløsninger
Kemiske opløsninger opstår, når et stof bringes i kontakt med en væske, og molekylerne interagerer med væskens molekyler. Hvis denne vekselvirkning resulterer i et lavere energiniveau, opløses stoffet. I nogle tilfælde opløses stoffet kun delvist, så nogle molekyler reagerer med væsken, mens andre forbliver uopløst og kan ses som bundfald. Selv små mængder stof indeholder ufatteligt mange molekyler, hvilket gør det umuligt at følge de enkelte molekyler. Derfor anvender kemikere ofte statistiske størrelser, som opløselighed, til at beskrive stoffets evne til at opløses. Opløselighed er et makroskopisk mål for, hvor stor en del af stoffets molekyler, der reagerer med væsken.
Både gasser, væsker og faste stoffer kan opløses i hinanden, hvilket skaber forskellige typer opløsninger. Eksempler omfatter danskvand (gas i væske), vin (væske i væske), saltvand (fast stof i væske) og legeringer som rustfrit stål (fast stof i fast stof). Mange opløsninger forekommer i hverdagen, fx øl, hvor alkohol, malt og CO₂ er opløst i vand.
I praksis anvendes opløsninger ofte i kemiske processer og laboratorier. Nogle stoffer som natriumklorid og sukker opløses let i vand, mens andre, som sølvchlorid (AgCl), er svært opløselige og kræver specifikke betingelser. For at kontrollere en opløsning er det vigtigt at kende både stoffets opløselighed og koncentration, hvilket kan bestemmes gennem forskellige kemiske målemetoder.

Måling af koncentration
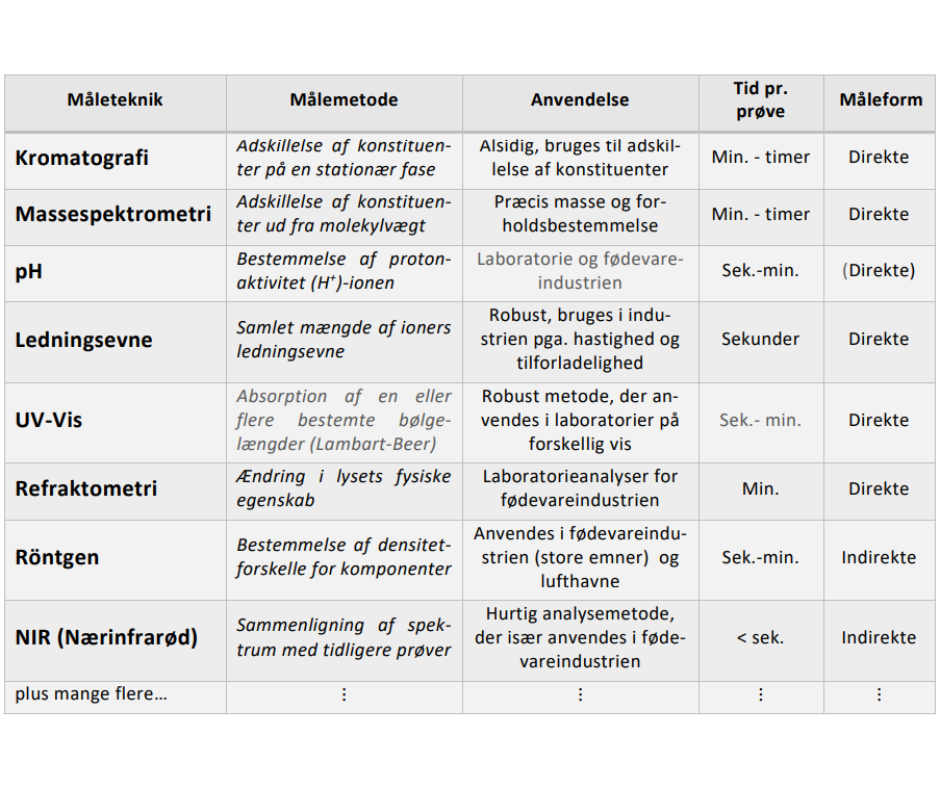
Koncentrationsbestemmelse er en analytisk metode, hvor mængden af en bestemt komponent, kaldet en konstituent, bestemmes i en blanding af flere stoffer. Et eksempel er maltsukker i øl, som findes opløst i vand sammen med humle og gær. Metoden anvendes bredt både i hverdagen og i industrien, hvor præcise koncentrationer har stor betydning for kvalitet, sikkerhed og funktion.
Et velkendt eksempel fra hverdagen er blodsukkermåling hos personer med diabetes. Her anvendes en enzymatisk metode, hvor glukose omdannes til en elektrisk strøm. Ved at måle spænding og strøm kan den samlede elektriske ladning beregnes, og ud fra dette estimeres stofmængden i blodet. Resultatet udtrykkes typisk som mol per liter (mol/L), hvilket giver et præcist mål for blodsukkerkoncentrationen. Denne information er afgørende for korrekt dosering af insulin, så kroppen kan fungere optimalt.
For at opnå pålidelige resultater skal metoden være selektiv og/eller måle på en prøve med få forstyrrende konstituenter. Koncentrationsbestemmelse kan udføres med mange forskellige teknikker, fra enzymatiske metoder til fysiske målinger som flydevægt. Hver metode har sine styrker og begrænsninger, og forståelse af disse er nødvendig for korrekt fortolkning af resultater. Formålet er altid at kunne bestemme koncentrationen nøjagtigt og reproducerbart, hvilket er afgørende i både forskning, produktion og sundhedssektoren.
Læs mere her
SI enhederne
Læs mere om naturkonstanter, SI-enhederne og deres definitioner samt afledte enheder.
Specifikke målemetoder
Dyk ned i specifikke målemetoder indenfor
- geometri
- masse
- temperatur
- og meget mere.
DFMs ydelser
Læs mere om vores ydelser indenfor
- målinger og kalibreringer
- konsulentarbejde
- projektsamarbejde og forskning
- kurser
- og meget mere
